一、STR的概念
短串联重复序列(short tandem repeat, STR),又称微卫星 DNA,是人类基因组中广泛存在的一类DNA序列。其核心重复单元通常由2-6个碱基对组成(如图1),在基因组中呈串联重复排列。
.png)
图1 STR结构示意图
STR主要分布于非编码区,约占人类基因组的3%。这类序列具有高度多态性,即不同个体同一STR位点上的重复次数存在显著差异,这使得STR成为区分供者与受者细胞的理想遗传标记。正因如此,可通过分析供、受者特异性STR片段的峰面积比值(图2),计算出供者细胞所占比例(即嵌合率),从而准确评估嵌合状态,实现移植后植入与复发情况的动态监测。
.png)
图2 受者、供者、移植后STR重复数峰图
二、STR 常见检测方法
STR的检测技术多样,下表总结了常见的STR检测技术及其特点:
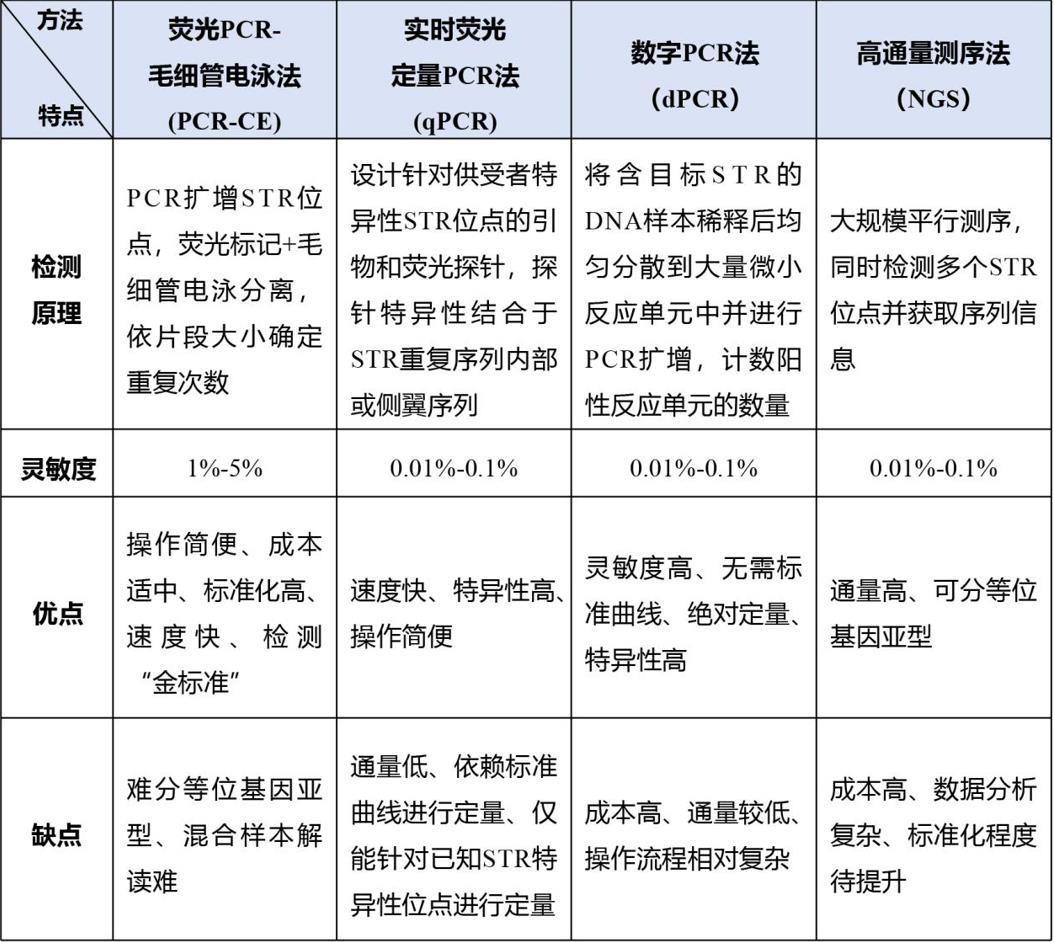
注:荧光PCR-毛细管电泳法为嵌合率检测金标准,适用于绝大多数异基因造血干细胞移植(allo-HSCT)患者;灵敏度不足时(如需检测<1% 的微小残留),可联合 qPCR、数字PCR或NGS技术。
三、STR检测报告解读
下图为一份移植供体细胞嵌合率的检测报告(图3),包含以下主要内容:
.png)
1. STR位点:对应图中第1列。研究结果显示,这些位点组合能显著降低随机匹配率,提高个体识别能力(图4)。
.png)
图4 人类染色体常见STR 标记位点分布图
2. 受者移植前后及供者STR重复次数:对应图中第2-4列。STR具有高度多态性和遗传稳定性,不同个体在同一位点的重复次数不同。移植后,若受者的STR位点出现供者特有的重复次数(如报告中受者移植后D18S51位点变为16, 18),提示供者细胞已在受者体内定植、增殖。
3. 嵌合率:通过专业软件分析供、受者特异性STR片段的峰面积比值,可计算出供者细胞占比,进而获得嵌合率来评估嵌合状态,为临床提供重要依据。
4. 嵌合状态:下表总结了供者细胞嵌合率对应的嵌合状态。
.png)
四、STR检测时机与样本选择
1. STR检测时机:
① 根据2001年国际共识1建议:对于移植中采用 T 细胞清除、非清髓 / 减低强度预处理方案,或使用新型移植物抗宿主病(GVHD)预防方案,应在移植后 1、3、6、12个月进行监测;而在非清髓移植早期,建议每 2~4 周检测一次;而针对非恶性血液肿瘤的移植,嵌合状态检测一般于移植后 1、2、3个月进行。
② 根据2025年国际共识2建议:推荐移植后前6个月每月检测1次全血嵌合状态,其中在移植后第 60 天、第 100 天可同时进行 T 细胞亚群(CD3)和髓系细胞亚群(CD15)的分型嵌合检测,术后6个月至1年每2个月检测1次,术后第2年每3个月检测1次。
2. STR检测的样本选择:
① 优先选择外周血,易获取且能反映全身造血嵌合状态。
② 骨髓样本用于疑似髓系复发时的精准评估,其造血干细胞比例更高,利于发现早期髓系异常。
③ 建议同步检测T细胞、CD34+细胞等亚群嵌合率,提高复发/排斥预警特异性,尤其对急性白血病、MDS患者价值突出。
五、STR检测临床意义
STR嵌合率检测是异基因造血干细胞移植(allo-HSCT)后临床管理的核心环节,其应用贯穿植入评估、并发症预警、治疗决策指导等全流程:
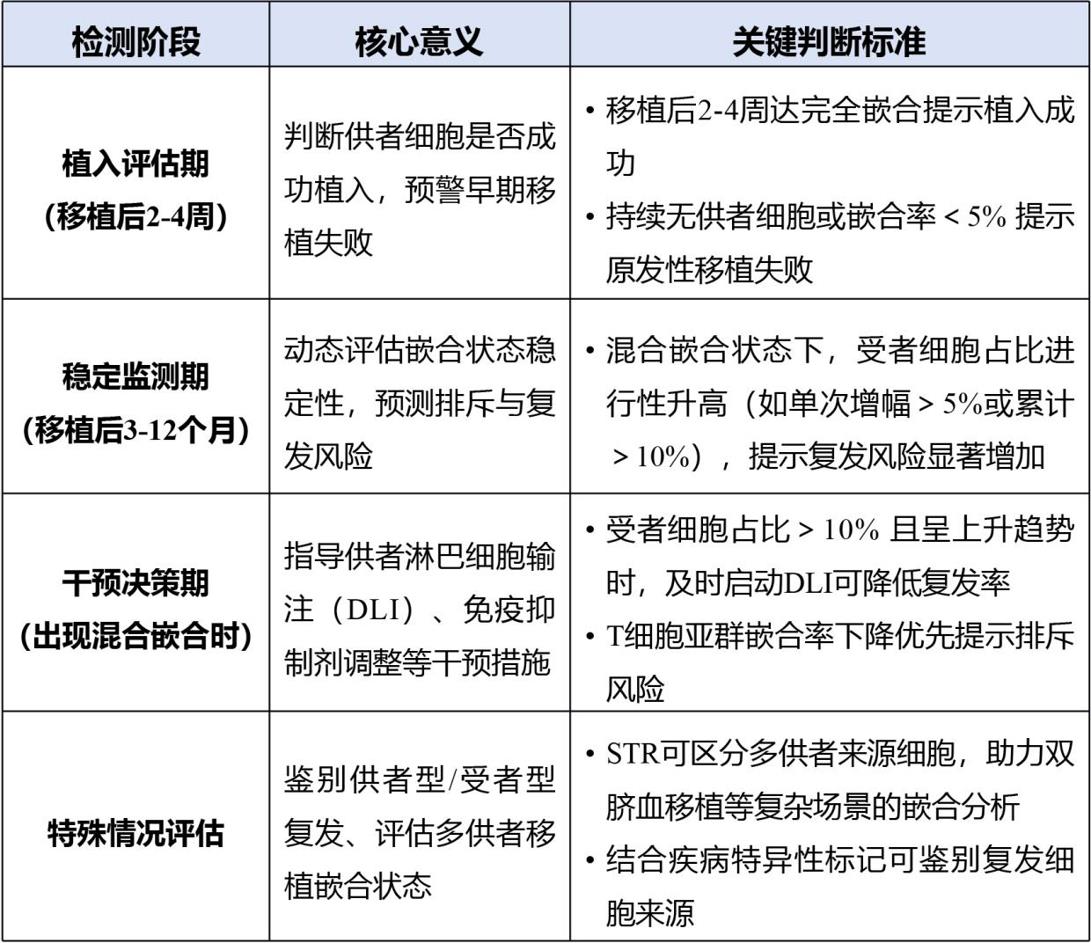
需注意:完全嵌合并非绝对“安全信号”,需结合疾病类型(如急性白血病需警惕分子残留病);混合嵌合需区分“稳定型”(低风险)与“进展型”(高风险),进展型需立即干预。
小结
STR嵌合率分析能够动态监测造血植入状态,及时提示复发或排斥风险,并指导临床决策。选择适宜的检测方法、规范采样时机与标本类型,并结合疾病特点与嵌合动态进行综合解读,是使其在异基因造血干细胞移植后管理中发挥核心作用的关键。
见康华美提供多项STR检测项目
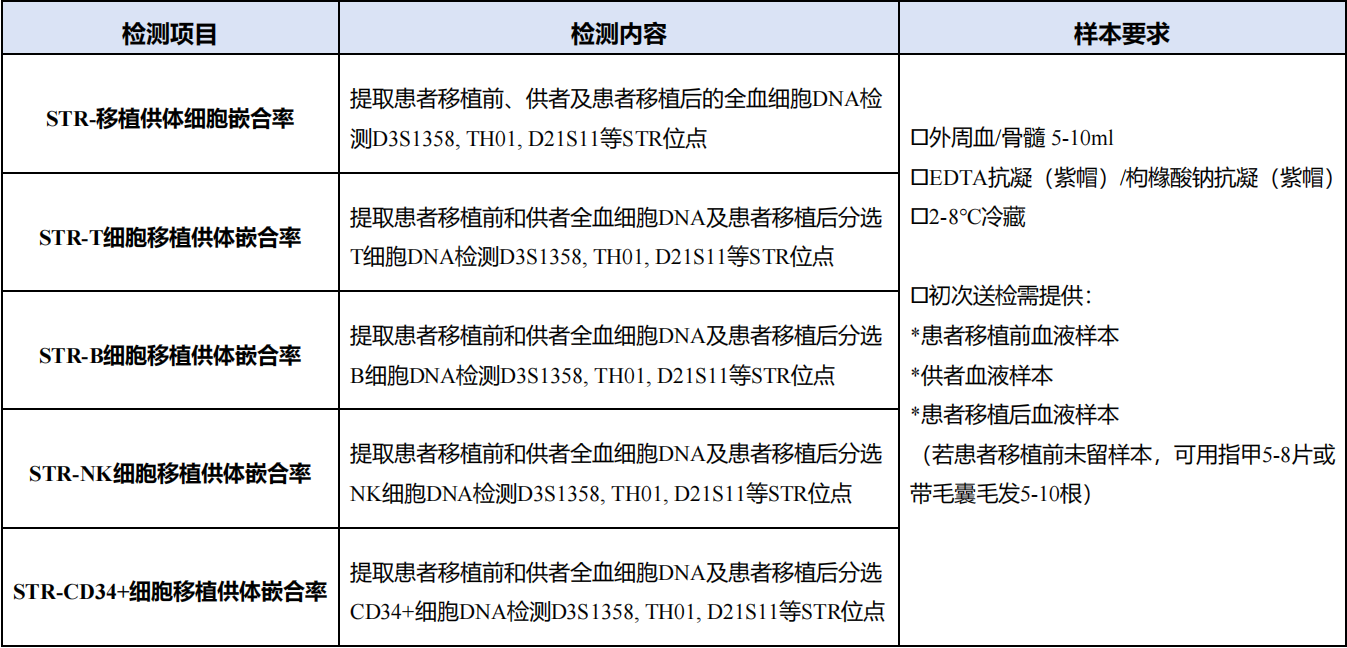
注:具体临床应用请遵循相关指南。
参考文献
1. Antin JH, Childs R, Filipovich AH, Giralt S, Mackinnon S, Spitzer T, Weisdorf D. Establishment of complete and mixed donor chimerism after allogeneic lymphohematopoietic transplantation: recommendations from a workshop at the 2001 Tandem Meetings of the International Bone Marrow Transplant Registry and the American Society of Blood and Marrow Transplantation. Biol Blood Marrow Transplant. 2001;7(9):473-85.
2. Andrew Clark, et al. UK recommendations for chimerism testing and monitoring following allogeneic haematopoietic stem cell transplantation (HSCT): Best practice consensus guidelines from the British Society for Blood and Marrow Transplant and Cellular Therapies (BSBMTCT), NHS England Genomic Laboratory Hub (GLH) Haematological Malignancies Working Group, UK Cancer Genetics Group (UKCGG) and the UK National External Quality Assessment Service for Leucocyte Immunophenotyping (UK NEQAS LI)[J].Br J Haematol. 2025 Nov;207(5):1802-1814.
3. Sureda A, et al. Harmonizing definitions for hematopoietic recovery, graft rejection, graft failure, poor graft function, and donor chimerism in allogeneic hematopoietic cell transplantation: a report on behalf of the EBMT, ASTCT, CIBMTR, and APBMT. Bone Marrow Transplant. 2024 Jun;59(6):832-837.
4. Almudena Navarro-Bailón, et al. Short Tandem Repeats (STRs) as Biomarkers for the Quantitative Follow-Up of Chimerism after Stem Cell Transplantation: Methodological Considerations and Clinical Application[J]. Genes (Basel).2020 Aug 25;11(9):993.
5. Dumache R, et al. Chimerism Monitoring by Short Tandem Repeat (STR) Markers in Allogeneic Stem Cell Transplantation [J]. Clin Lab. 2018 Sep 1;64(9):1535-1543.
6. Blouin AG, et al. A Practical Guide To Chimerism Analysis: Review of The Literature and Testing Practices Worldwide[J]. Hum Immunol. 2021 Nov;82(11):838-849.
7. Saori Miura, et al. Prospects and potential for chimerism analysis after allogeneic hematopoietic stem cell transplantation[J]. Cells. 2024 Jun 6;13(11):993.